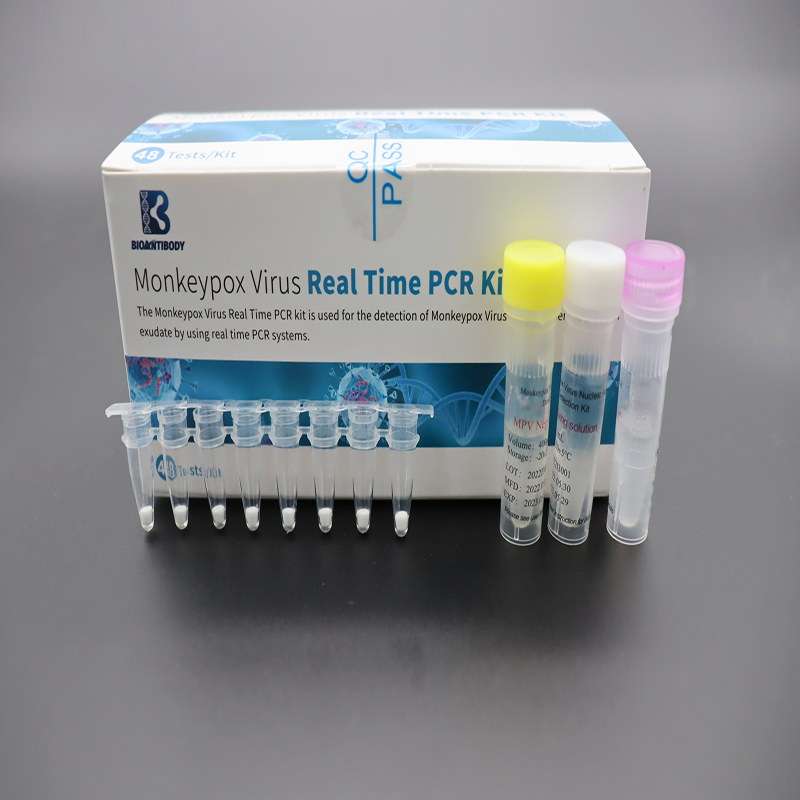
Kit per PCR in tempo reale del virus del vaiolo delle scimmie
Dettagli del prodotto
Uso previsto
Viene utilizzato per il rilevamento del virus del vaiolo delle scimmie in campioni di siero umano o di essudato di lesioni utilizzando sistemi PCR in tempo reale.
Principio della prova
Questo prodotto è un sistema di analisi PCR in tempo reale Taqman® basato su sonda fluorescente.Primer e sonde specifici sono progettati per il rilevamento del gene F3L del virus del vaiolo delle scimmie.Il controllo interno mirato al gene umano conservato monitora la raccolta dei campioni, la manipolazione dei campioni e il processo PCR in tempo reale per evitare risultati falsi negativi.Il kit è un sistema liofilizzato completamente premiscelato, che comprende i materiali necessari per il rilevamento del virus del vaiolo delle scimmie: enzima di amplificazione dell'acido nucleico, enzima UDG, tampone di reazione, primer specifico e sonda.
Contenuti principali
I componenti forniti sono elencati nella tabella.
| Componenti | Pacchetto | Ingrediente |
| Virus del vaiolo delle scimmiePremiscela liofilizzata | 8 strisce di provette per PCR× 6 buste | Primer, sonde, miscela dNTP/dUTP, Mg2+, Taq DNA polimerasi, enzima UDG |
| Controllo positivo MPV | Provetta da 400 μL×1 | Sequenze di DNA contenenti il gene bersaglio |
| Controllo negativo monovolume | Provetta da 400 μL×1 | Sequenze di DNA contenenti segmenti di gene umano |
| Soluzione dissolvente | 1 ml×1 provetta | Stabilizzatore |
| Certificato di conformità | 1 pezzo | / |
Flusso operativo
1. CampioneCollezione:I campioni devono essere raccolti in provette sterili in conformità
con specifiche tecniche standard.
2. Preparazione dei reagenti (area di preparazione dei reagenti)
Estrarre i componenti del kit, bilanciarli a temperatura ambiente per l'uso in standby.
3. Elaborazione dei campioni (area di elaborazione dei campioni)
3.1 Estrazione dell'acido nucleico
Si consiglia di prelevare 200μL di campioni liquidi, controllo positivo e controllo negativo per l'estrazione dell'acido nucleico, secondo i requisiti e le procedure corrispondenti dei kit di estrazione del DNA virale.
3.2 Dissoluzione della polvere liofilizzata e aggiunta del modello
Preparare la premiscela liofilizzata del virus del vaiolo delle scimmie in base al numero di campioni.Un campione necessita di una provetta PCR contenente polvere premiscelata liofilizzata.Il controllo negativo e il controllo positivo devono essere trattati come due campioni.
(1) Aggiungere 15μL di soluzione dissolvente in ciascuna provetta PCR contenente la premiscela liofilizzata, quindi aggiungere rispettivamente 5μL di campioni estratti/controllo negativo/controllo positivo in ciascuna provetta PCR.
(2) Coprire bene le provette PCR, muovere manualmente le provette PCR finché la polvere liofilizzata non è completamente dissolta e miscelata, raccogliere il liquido sul fondo delle provette PCR mediante centrifugazione istantanea a bassa velocità.
(3) Se si utilizza un comune strumento PCR in tempo reale per il rilevamento, trasferire direttamente le provette PCR nell'area di amplificazione;se si utilizza BTK-8 per il rilevamento, è necessario eseguire le seguenti operazioni: trasferire 10 μL di liquido dalla provetta PCR al pozzetto del chip di reazione di BTK-8.Una provetta PCR corrisponde a un pozzetto sul chip.Durante l'operazione di pipettaggio, assicurarsi che la pipetta sia verticale di 90 gradi.I puntali delle pipette con barriera aerosol devono essere posizionati al centro del pozzetto con forza moderata e smettere di spingere la pipetta quando raggiunge la prima marcia (per evitare bolle).Dopo aver riempito i pozzetti, estrarre la membrana del chip di reazione per coprire tutti i pozzetti e trasferire il chip nell'area di rilevamento dell'amplificazione.
4. Amplificazione PCR (area di rilevamento)
4.1 Mettere le provette per PCR/il chip di reazione nel serbatoio di reazione e impostare i nomi di ciascun pozzetto di reazione nell'ordine corrispondente.
4.2 Impostazioni di rilevamento della fluorescenza: (1) Virus del vaiolo delle scimmie (FAM);(2) Controllo interno (CY5).
4.3 Eseguire il seguente protocollo di ciclismo
Protocollo di ABI7500, Bio-Rad CFX96, SLAN-96S, QuantStudio:
| Passi | Temperatura | Tempo | Cicli | |
| 1 | Pre-denaturazione | 95 ℃ | 2 minuti | 1 |
| 2 | Denaturazione | 95 ℃ | 10 secondi | 45 |
| Ricottura, estensione, acquisizione della fluorescenza | 60 ℃ | 30 secondi | ||
Protocollo BTK-8:
| Passi | Temperatura | Tempo | Cicli | |
| 1 | Pre-denaturazione | 95 ℃ | 2 minuti | 1 |
| 2 | Denaturazione | 95 ℃ | 5 secondi | 45 |
| Ricottura, estensione, acquisizione della fluorescenza | 60 ℃ | 14 secondi | ||
5. Analisi dei risultati (fare riferimento al manuale utente dello strumento)
Dopo la reazione, i risultati verranno salvati automaticamente.Fare clic su "Analizza" per analizzare e lo strumento interpreterà automaticamente i valori Ct di ciascun campione nella colonna dei risultati.I risultati dei controlli negativi e positivi devono essere conformi al seguente "6. Controllo di qualità".
6. Controllo di qualità
6.1 Controllo negativo: assenza di Ct o Ct>40 nel canale FAM, Ct≤40 nel canale CY5 con curva di amplificazione normale.
6.2 Controllo positivo: Ct≤35 nel canale FAM con curva di amplificazione normale, Ct≤40 nel canale CY5 con curva di amplificazione normale.
6.3 Il risultato è valido se tutti i criteri di cui sopra sono soddisfatti.In caso contrario, il risultato non è valido.
Interpretazione dei risultati
Sono possibili i seguenti risultati:
| Valore Ct del canale FAM | Valore Ct del canale CY5 | Interpretazione | |
| 1# | Nessun Ct o Ct>40 | ≤40 | Negativo al virus del vaiolo delle scimmie |
| 2# | ≤40 | Qualsiasi risultato | Positivo al virus del vaiolo delle scimmie |
| 3# | 40~45 | ≤40 | Ritestare;se è ancora 40~45, segnala come 1# |
| 4# | Nessun Ct o Ct>40 | Nessun Ct o Ct>40 | Non valido |
NOTA: Se si verificano risultati non validi, il campione deve essere raccolto e testato nuovamente.
Informazioni sull'ordine
| nome del prodotto | Gatto.NO | Misurare | Campione | Data di scadenza | Trans.& Sto.Temp. |
| Kit per PCR in tempo reale del virus del vaiolo delle scimmie | B001P-01 | 48 test/kit | Siero/Essudato della lesione | 12 mesi | -25~-15℃ |